OSTALI SEMINARSKI RADOVI
IZ MEDICINE |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
HEPATITIS C
Virus hepatitisa C (HCV) otkriven je
1989. godine. Njegovim je otkrićem razjašnjena etiologija velikog broja
posttransfuzijskog hepatitisa dotad nepoznatog uzroka. Specifična anti-HCV
protutijela nađena su u 70-90% bolesnika s posttransfuzijskim non-A, non-B
hepatitisom.
Slika 1. Virus hepatitisa C (elektronska mikroskopija)
Zbog slicne grade genoma i polipeptida s drugim humanim flavivirusima, HCV je svrstan u porodicu Flaviviridae, rod Hepacivirus.
2. GRADJA I UMNOŽAVANJE VIRUSA HEPATITISA C
2.1. Građa virusa hepatitisa C
Virusna čestica je sferična oblika, velicine oko 60 nm. Nukleokapsida
je promjera 30 nm, ovijena lipidnom ovojnicom na kojoj se nalaze glikoproteinski
izdanci.
Genom čini jednolančana pozitivna (+) RNA velicine ~9.6 nukleotida (slika 2) koja sadrži tri regije: a) kratku nekodirajuću regiju na 5' kraju, b) veliko otvoreno područje kodiranja (engl. open reading frame; ORF) i c) kratku nekodirajuću regiju na 3' kraju.
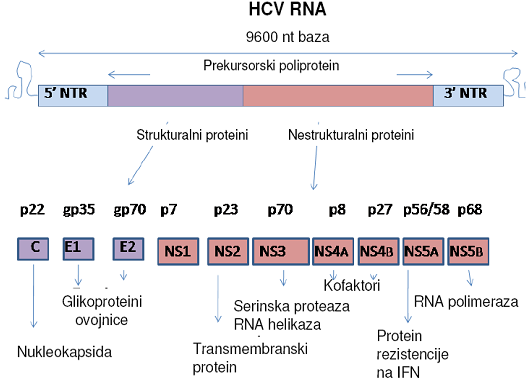
Slika 2. Organizacija genoma virusa hepatitisa C
Produkt prevođenja ORF je poliprotein koji se posttranslacijski cijepa pomoću virusnih i staničnih proteaza u 10 proteina. Oni uključuju tri strukturna proteina: protein kapside (C) i dva glikoproteina ovojnice (E1 i E2), pet nestrukturnih proteina (NS3, NS4A, NS4B, NS5A i NS5B), većinom enzima koji sudjeluju u procesu umnožavanja te dva proteina (p7 i NS2) koja imaju ulogu u sastavljanju virusne čestice (tablica 1). Glikoproteini E1 i E2 građeni su u obliku heterodimera. Prvih 27 aminokiselina glikoproteina E2 tvore tzv. Hipervarijabilnu regiju (HVR-1) koja predstavlja najvarijabilniju regiju genoma i posjeduje epitope koji izazivaju stvaranje neutralizirajucih protutijela.
Tablica 1. Proteini HCV i njihova funkcija tijekom umnožavanja virusa
2.2. Umnožavanje virusa hepatitisa C
Umnožavanje HCV započinje vezanjem virusa za stanicne receptore (slika 3). Iako stanični receptori nisu točno poznati, na površini stanica dokazane su razlicite molekule koje se vežu s HCV: CD81, lipoproteinski receptor niske gustoce (LDL), humani čistački receptor tipa B (engl. scavenger receptor B type; SR-BI), lektini C-tipa: DC-SIGN (engl. dendritic cell-specific intercellular adhesion molecule-3-grabbing non integrin) i L-SIGN (engl. liver/lymph nodespecific intercellular adhesion molecule-3-grabbing integrin), a u novije vrijeme otkriven je i klaudin-1.
Neki se receptori nalaze na razlicitim stanicama, dok su drugi specificni za pojedinu vrstu stanica. CD81 je transmembranski receptor koji pripada porodici tetraspanina, a nalazi se na mnogim humanim stanicama, ukljucujuci hepatocite i B-limfocite. CD81 se veže s HCV E2, ali je za ulazak virusa u stanicu potreban i sekundarni receptor odnosno koreceptor. SR-BI je lipoproteinski receptor visoke gustoce koji se nalazi u visokoj koncentraciji na hepatocitima i veže s HCV E2. DC-SIGN se nalazi na dendritickim stanicama, a L-SIGN na endotelnim stanicama jetrenih sinusoida i limfnih čvorova. Oba receptora olakšavaju ulazak HCV u hepatocite, a vjerojatno i PMN. Ulazak HCV u stanicu pospješuju i druge molekule kao glikozaminoglikani - heparin i heparan sulfat.
Virus ulazi u stanicu receptorom posredovanom endocitozom. Zbog niskog pH u endosomu dolazi do konformacijskih promjena proteina ovojnice, fuzije virusa s membranom endosoma (djelovanjem E1) te otpuštanja RNA u citoplazmu. HCV RNA na 5’ kraju sadrži kompleksnu strukturu tzv. IRES (engl. internal ribosomal entry site) koja se veže na 40S podjedinicu ribosoma i omogućuje početak translacije.
Slika 3. Umnožavanje virusa hepatitisa C
a) vezanje HCV za stanicni receptor i ulazak u stanicu; (b) svlacenje
HCV i otpuštanje u citoplazmu; (c) prevodenje u poliprotein pomocu IRES;
(d) replikacija RNA; (e) sastavljenje HCV; (f) sazrijevanje HCV i izlazak
iz stanice.
Umnožavanje HCV RNA odvija se na specificnoj tzv. mrežastoj membrani.
Genom djeluje kao mRNA i prevodi se u poliprotein. Strukturni se proteini
cijepaju pomoću staničnih proteaza (signalna peptidaza), a nestrukturalni
proteini pomoću virusne NS2-NS3 proteaze i NS3 serinske proteaze (20).
Nestrukturalni proteini NS3-NS5B se spajaju i tvore kompleks replikaze
na intracitoplazmatskim membranama koja kodira sintezu negativnog lanca
RNA, a on služi kao kalup za sintezu pozitivnog lanca genoma. Novosintetizirana
genomska RNA spaja se s proteinom kapside i tvori nukleokapsidu. Virus
dobiva ovojnicu pupanjem kroz intracelularne vezikule, a iz stanice se
oslobada egzocitozom ili lizom (slika 3).
2.3. Genotipovi virusa hepatitisa C
Izolati HCV iz različitih dijelova svijeta pokazuju značajnu genetsku
varijabilnost. Prema glavnom filogenetskom stablu postoji 6 genotipova
i više od 90 podtipova (slika 4).
Slika 4. Genotipovi virusa hepatitisa C
Pojedini se genotipovi u nukleotidnom slijedu razlikuju 31-33%, dok se podtipovi razlikuju oko 20-25%. Osim toga, HCV, kao i drugi RNA-virusi, pokazuje visok stupanj spontanih mutacija (10-5 pogrešaka/nt). Virusna RNA polimeraza nema sposobnost prepoznavanja pogrešno umetnutih nukleotida tijekom umnožavanja niti djelotvornog "popravka" RNA što dovodi do brojnih genomski razlicitih varijanti istog virusa u jednom domacinu tzv. "kvazispecijesa". Kvazispecijesi se razlikuju u nukleotidnom slijedu do 10%. Neki su genotipovi široko rasprostranjeni (1a, 1b, 2a i 2b) dok se drugi (5a i 6a) pojavljuju na ograničenim geografskim područjima (slika 5).
Slika 5. Raspodjela genotipova virusa hepatitisa C
Osim karakteristične geografske rasprostranjenosti, pojedini su podtipovi
nađeni u specifičnim rizičnim skupinama. U Europi, Americi i vecem dijelu
Azije, 40-80% HCV infekcija uzrokovano je genotipom 1. Genotip 1 ima dva
glavna podtipa: 1a koji je najcešci u Sjevernoj Americi i 1b koji je rasprostranjen
na podrucju Europe i Sjeverne Amerike u starijih osoba te osoba inficiranih
transfuzijom krvi. Genotip 2 prevladava na području Mediterana i u Aziji.
Genotip 3 (podtip 3a) raširen je u i.v. korisnika droga na području Europe,
genotip 4 na Srednjem Istoku, genotip 5 gotovo isključivo u Južnoj Africi
te genotip 6 u jugoistocnoj Aziji (Hong Kong, Makau i Vijetnam).
Istraživanje provedeno na području Hrvatske pokazalo je da su najčešci genotipovi 1 (58,8%) i 3 (35,6%). Učestalost genotipova 2 i 4 je niska (2,2%, odnosno 3,4%), dok genotipovi 5 i 6 nisu dokazani. Najzastupljeniji podtip je 1b, dokazan u 37,4% te 1a u 13,1% bolesnika.
3. EPIDEMIOLOGIJA INFEKCIJE VIRUSOM HEPATITISA C
3.1. Seroprevalencija infekcije virusom hepatitisa C u svijetu
Infekcija s HCV zabilježena je u gotovo svim dijelovima svijeta. Prema
podacima Svjetske Zdravstvene Organizacije, procjenjuje se da je oko 170-200
milijuna ljudi, odnosno 3% svjetske populacije, zaraženo s HCV (tablica
2), iako je stvarna prevalencija vjerojatno viša jer vecina infekcija
protjece asimptomatski te ostaje neprepoznata. Smatra se da se godišnje
s HCV zarazi oko tri do četiri milijuna ljudi.
Tablica 2. Procijenjena distribucija broja osoba zaraženih virusom hepatitisa C
Seroprevalencija HCV infekcije razlikuje se po regijama (slika 6). Prema podacima iz literature, područja s najnižom prevalencijom (0,1%) su Velika Britanija i Skandinavija (29). Nešto viša prevalencija (0,2-0,5%) zabilježena je u SAD, zapadnoj Europi i Australiji. Srednje visoku prevalenciju HCV infekcije (1-5%) imaju istocna Europa, Brazil, Srednji Istok i Indijski potkontinent, a država s najvišom prevalencijom (17-26%) je Egipat (slika 6). U Egiptu se prijenos HCV infekcije povezuje s višestrukim korištenjem staklenih šprica tijekom nacionalne kampanje vezane uz borbu protiv shistosomijaze koja se provodila od 1960. do 1987. godine. Na slici 7 prikazana je seroprevalencija HCV infekcije u Europi.
Slika 6. Seroprevalencija infekcije virusom hepatitisa C u svijetu
Slika 7. Seroprevalencija infekcije virusom hepatitisa C u Europi
Uz geografske razlike, u prevalenciji HCV infekcije postoje i dobno specificne razlike. Npr. SAD, Australija, Italija i Španjolska pripadaju skupini država s podjednakom prevalencijom HCV infekcije (1-1,9%) (32). U SAD, najviša prevalencija HCV (dvije trećine svih infekcija) zabilježena je u dobnim skupinama od 30-49 godina. Nasuprot tome, u Italiji i Španjolskoj prevalencija hepatitisa C se povecava s dobi te je najveci broj zaraženih u dobi iznad 50 godina. U nekim zemljama, npr. Italiji, Japanu i Kini, postoje hiperendemska područja u kojima je prevalencija HCV infekcije cak dvadeset puta viša nego u općoj populaciji te dvostruko viša od prevalencije u istim dobnim skupinama u ostalim dijelovima države.
3.2. Putevi prijenosa infekcije virusom hepatitisa C
Glavni put prijenosa HCV je perkutana izloženost zaraženoj krvi. Rizik
prijenosa je najveći nakon obilne izravne (transfuzija krvi i krvnih derivata
od inficiranog davaoca) ili opetovane perkutane ekspozicije (uporaba kontaminiranog
pribora pri i.v. primjeni droga). Opisana je i učestalija pojava HCV infekcije
u osoba koje rabe kokain za ušmrkavanje, vjerojatno zbog zajednicke uporabe
pribora kontaminiranog krvlju. Srednje velik rizik prijenosa HCV imaju
osobe u kojih je došlo do manje, ali ponovljene perkutane ekspozicije
poput bolesnika na hemodijalizi. Nizak rizik postoji u osoba s inaparentnom
parenteralnom ili permukoznom ekspozicijom kao što su osobe u bliskom
obiteljskom kontaktu s inficiranom osobom. Prevalencija anti-HCV iznosi
do 98% u i.v. korisnika droga I bolesnika s hemofilijom, 20-30% u bolesnika
na hemodijalizi, 0,2-18% u općoj populaciji te 0,3-0,5% u dobrovoljnih
davatelja krvi.
U slučajevima sporadicnih perkutanih ekspozicija, poput onih u zdravstvenih djelatnika, učestalost infekcije ne prelazi 1% (43). Stopa prijenosa HCV infekcije nakon jednog uboda kontaminiranom injekcijskom iglom iznosi oko 3% (1-6%).
Uloga spolnog načina prijenosa HCV još uvijek nije potpuno razjašnjena, a podaci iz literature su kontroverzni. Na potencijalnu ulogu spolnog puta prijenosa upućuju podaci da je u podrucjima visoke HCV endemičnosti i visoke učestalosti spolno prenosivih bolesti (SPB), prevalencija HCV niska u djece i adolescenata, a povecava se s dobi. HCV-RNA dokazana je u sjemenoj tekucini, vaginalnom i cervikalnom sekretu. Neki su radovi pokazali da heteroseksualni partneri HCV-pozitivnih osoba imaju veću incidenciju HCV infekcije od opće populacije, dok drugi nisu našli veću prevalenciju HCV u osoba koje su u monogamnoj heteroseksualnoj vezi s HCV-pozitivnim partnerom. Međutim, čini se da je u osoba rizičnog spolnog ponašanja (prodavateljice seksualnih usluga, osobe koje često mijenjaju spolne partnere) ucestalost HCV viša, iako su i tu mišljenja podijeljena. Istraživanja seroprevalencije u homoseksualaca također su dala oprečne rezultate. Uloga mogućih kofaktora (npr. specifičnog spolnog ponašanja) u prijenosu HCV spolnim putem također nije razjašnjena.
Neki su radovi pokazali višu prevalenciju HCV u osoba sa SPB u anamnezi. Prisustvo SPB povećava vjerojatnost prijenosa HCV zbog oštecenja sluznice spolnih organa te smanjenja lokalne imunosti. Povecan rizik spolnog prijenosa HCV opisan je i u slucaju koinfekcije virusom HIV-a, vjerojatno zbog više razine HCV-RNA u bolesnika s HIV-infekcijom u odnosu na bolesnike inficirane samo s HCV, ali su i tu rezultati kontradiktorni.
Do perinatalnog prijenosa HCV dolazi u oko 5% slucajeva (0-25%), što ovisi o stupnju viremije majke u vrijeme poroda. Rizik prijenosa infekcije na novorodence je viši (5-36%) ukoliko je majka istodobno inficirana i virusom HIV-a. Iako je HCV izoliran iz majčinog mlijeka, nikada nije opisan prijenos infekcije dojenjem.
Prema podacima iz literature, u cak 30-50% zaraženih ne može se sa sigurnošcu utvrditi put prijenosa.
4. PATOGENEZA INFEKCIJE VIRUSOM HEPATITISA C
Hepatociti su primarno mjesto umnožavanja virusa i sadrže veliku kolicinu
HCV-RNA (108-1011 kopija/gram tkiva), što je dokazano in situ hibridizacijom.
Virus se nalazi u citoplazmi hepatocita i ne ugraduje se u genom stanice
domacina. Međutim, novije su imunohistokemijske studije pokazale da se
virus nalazi i u bilijarnom epitelu te mononuklearnim stanicama periferne
krvi, koje mogu poslužiti kao rezervoar za ponovnu reaktivaciju nakon
prestanka lijecenja. Umnožavanje virusa je vrlo brzo (~1012 virusnih čestica
na dan) s vremenom poluživota 3-5 sati.
Patogeneza jetrenog oštećenja najvjerojatnije je posljedica izravnog citopatskog učinka virusnih proteina i imunoloških mehanizama posredovanih citotoksicnim limfocitima i citokinima.
5. KLINICKA SLIKA INFEKCIJE VIRUSOM HEPATITISA C
Hepatitis C pojavljuje se u obliku akutne ili kronične infekcije. Inkubacija
iznosi prosječno 6-7 tjedana.
Akutni hepatitis C
Akutna HCV infekcija u većini slučajeva (>80%) protječe asimptomatski. Bolest se klinički očituje nespecifičnim simptomima - umorom, slabošcu, mučninom te bolovima u desnom gornjem abdominalnom kvadrantu, a ikterus se javlja u 20-30% oboljelih. Fulminantni tijek akutnog hepatitisa C iznimno je rijedak. Teži se oblici bolesti viđaju u osoba s alkoholnom bolesti jetre te HIV i HBV koinfekcijom. Najčešci prirodni tijek infekcije je asimptomatski prijelaz u kronični hepatitis.
Kronicni hepatitis C
Kronični hepatitis karakterizira perzistencija HCV-RNA u krvi dulje od šest mjeseci. Većina autora smatra da oko 80% zaraženih osoba razvija perzistentnu infekciju s dugotrajnom viremijom koja može progredirati do fibroze i ciroze jetre (oko 25%) te hepatocelularnog karcinoma (1-7%). Kao predisponirajuci faktori za razvoj progresivne bolesti jetre navode se starija dob pri stjecanju infekcije (>40 godina), muški spol i prekomjerno konzumiranje alkohola (tablica 3).
Tablica 3. Rizični faktori za razvoj progresivne bolesti jetre
Većina bolesnika s kroničnim hepatitisom C je asimptomatska. Najčešci simptom je kronični umor, artralgija i mijalgija, medutim njihovo prisustvo ne korelira s težinom bolesti.
Okultni hepatitis C
Castillo i sur. opisali su 2004. godine novi oblik hepatitisa C tzv.
“okultni hepatitis C” koji karakterizira prisustvo HCV-RNA u jetri uz
negativne serološke biljege infekcije (anti-HCV i HCV-RNA u serumu). Osim
u jetri, u 70% bolesnika HCV-RNA je dokazana i u mononuklearima periferne
krvi.
Mnoge su bolesti izvan jetre izravno ili neizravno povezane s kroničnom
HCV infekcijom (tablica 4).
Tablica 4. Ekstrahepaticke manifestacije HCV infekcije
Oko 40-70% bolesnika s kroničnom HCV infekcijom razvije ekstrahepaticke simptome koji su često prvi znak infekcije budući da većina bolesnika nema znakove jetrene bolesti. Ekstrahepaticka tkiva mogu služiti kao rezervoar virusa te imaju ulogu kako u perzistenciji tako i u reaktivaciji HCV. Uz hepatotropizam, HCV pokazuje izraziti limfotropizam koji je odgovoran za mnoge ekstrahepaticke simptome bolesti. Imunološke su prirode i uključuju krioglobulinemiju, limfoproliferativne, kožne te endokrinološke simptome.
Miješana krioglobulinemija dovodi do sistemskog vaskulitisa karakteriziranog odlaganjem cirkulirajucih krioglobulina koji se sastoje od poliklonskih IgG i monoklonskih IgM protutijela u malim krvnim žilama. Krioglobulini su dokazani u 19-50% bolesnika s HCV infekcijom. Krioprecipitati obicno sadrže velike kolicine HCV antigena i/ili anti-HCV protutijela. Kronicna HCV infekcija udružena je i s bolestima bubrega, posebno s membranoproliferativnim glomerulonefritisom koji je histološki obilježen odlaganjem depozita IgG i IgM te C3 komponente komplementa u glomerulima. HCV-RNA je dokazana u 81% bolesnika s membranoproliferativnim glomerulonefritisom. Non-Hodgkin limfomi se mogu pojaviti u perzistentnim oblicima krioglobulinemije (8-10%) ili kao zasebna bolest u bolesnika s kroničnom HCV infekcijom. Medutim, podaci o prisustvu HCV u malignim stanicama su kontradiktorni. Dok neke studije nisu detektirale HCV u stanicama limfoma, druge su dokazale prisustvo HCV-RNA u limfoidnim organima i koštanoj srži. Od drugih hematoloških bolesti, u bolesnika s HCV opisana je pojava gamopatije. Neki su autori dokazali povezanost gamopatije s genotipom HCV 2a/c.
Iako je povezanost HCV infekcije i bolesti štitnjace nejasna, hipotireoza je češca u bolesnika s HCV nego u općoj populaciji. Oko 13% bolesnika s HCV infekcijom razvije hipotireozu, a oko 25% ima detektabilna antitireoidna protutijela.
Opisane su i druge ekstrahepatičke komplikacije kao artritis, Sjogrenov sindrom, lihen planus, kardiomiopatija i idiopatska pulmonalna fibroza, no nema sigurnih dokaza o povezanosti tih bolesti s HCV infekcijom.
6. IMUNOLOŠKI ODGOVOR NA INFEKCIJU VIRUSOM HEPATITISA C
U većine HCV inficiranih razvija se aktivan imuni odgovor. Na to ukazuje
prisustvo anti-HCV protutijela, T i B-stanicni odgovor te ekstrahepaticke
manifestacije autoimune bolesti.
Nespecifični odgovor na HCV infekciju ukljucuje prirodnoubilacke (NK) stanice, aktivaciju komplementa, interferon te produkciju citokina. Aktivirane dendriticne stanice induciraju diferencijaciju naivnih T limfocita u virus specificne CD4+ i CD8+ limfocite T (78). Specifićni imuni odgovor ukljucuje staničnu (citotoksicni T-limfociti; CTL) i humoralnu imunost (protutijela).
Iako je HCV osjetljiv na interferon in vitro, novije su studije pokazale da HCV može interferirati s njegovom antivirusnom aktivnošcu. HCV može suprimirati intracelularnu produkciju interferona-a zbog inhibitornog ucinka pojedinih nestrukturnih proteina HCV (NS3-NS4A, NS5A) na sekreciju interferona. Takoder je dokazan inhibitorni učinak glikoproteina HCV na NK stanice. Vezanjem na površinu NK stanica, glikoproteini inhibiraju njihovu aktivaciju, sekreciju citokina i citotoksicnu aktivnost. In vitro studije pokazale su da NK stanice bolesnika s HCV infekcijom, za razliku od zdravih osoba, imaju smanjenu sposobnost aktivacije dendriticnih stanica.
HCV u većini slučajeva uzrokuje kroničnu infekciju. Točan mehanizam perzistencije virusa još uvijek nije poznat. Smatra se da su CD8+ limfociti T glavne antivirusne efektorske stanice u HCV infekciji (81, 82). Oni prepoznaju virusni antigen predočen molekulama HLA-razreda i na antigen-prezentirajucim stanicama (specifično pobuđivanje CD8+ limfocita) te na inficiranim hepatocitima. Nadalje, antivirusna aktivnost CD8+ limfocita T ukljucuje citotoksicnost i sekreciju antivirusnih citokina (interferon-g).
Tijekom akutne HCV infekcije s eliminacijom virusa, približno 4-8 tjedana nakon infekcije vidi se vrlo jaki multispecificni (na razlicite virusne epitope) CD8+ T stanični odgovor. Međutim, u ranoj fazi infekcije CD8+ limfociti ne mogu izlučivati antivirusne citokine kao interferon-g, stanje nazvano “zakoceni fenotip”. U kasnijoj fazi oni ponovno stječu sposobnost produkcije citokina što je povezano s brzim smanjenjem viremije i naposljetku eliminacijom virusa. Specificni CD8+ i CD4+ limfociti T perzistiraju godinama nakon infekcije, čak dulje od humoralnog odgovora. Nasuprot tome, u perzistentnoj HCV infekciji odgovor CD8+ limfocita je znatno slabiji i nije multispecifican.
Osim CD8+ limfocita T, za uspješnu eliminaciju HCV potrebni su CD4+ limfociti T kako bi održali CD8+ T stanicni odgovor. U kronicnoj je HCV infekciji odgovor CD4+ slab ili čak izostaje, a takoder je oštecena i njihova funkcija tj. smanjena je produkcija IL-2.
Neki HCV proteini pokazuju imunomodulacijski ucinak. Opaženo je da protein kapside (C) djeluje na diferencijaciju limfocita T i njihovu funkciju. C protein veže se na receptore za komplement na površini makrofaga i limfocita T što smanjuje produkciju IL-2 te i proliferaciju limfocita T.
Novije su studije dokazale postojanje regulatornih CD4+CD25+ T stanica u bolesnika s kroničnom HCV infekcijom koje imaju važnu ulogu u supresiji specifičnog imunog odgovora (84-86). Studije in vitro pokazale su da te stanice suprimiraju proliferaciju specifičnih CD4+ i CD8+ limfocita T kao i lucenje interferona-g što pospješuje perzistenciju virusa.
Tijekom HCV infekcije opažene su modifikacije T i B epitopa što omogućuje virusu da izbjegne imunološkom sustavu. Jedan od najvažnijih mehanizama perzistencije su česte mutacije u podrucju HVR-1 te nastanak kvazispecijesa što omogućuje HCV uspješno izbjegavanje imunološkom odgovoru.
Osim hepatocita, HCV inficira limfocite T i B te oštecuje njihovu funkciju.
Iako se tijekom HCV infekcije stvaraju neutralizirajuca antitijela, ona su specifična za soj virusa te ne omogućuju potpunu zaštitu od reinfekcijem homolognim ili heterolognim virusom, a pokusne infekcije u majmuna upucuju na to da imunost nije doživotna.
7. VIROLOŠKA DIJAGNOSTIKA INFEKCIJE VIRUSOM HEPATITISA C
Dijagnostika hepatitisa C provodi se detekcijom HCV antigena, HCV-RNA
te anti-HCV protutijela.
7.1. Serološka dijagnostika infekcije virusom hepatitisa C
Protutijela usmjerena na različite antigene HCV gotovo su uvijek prisutna u kroničnoj HCV infekciji. Samo u malom broju bolesnika (5-10%), najčešce imunokompromitiranih ne stvaraju se detektabilne razine protutijela ili je njihova produkcija usporena.
Testovi za dokazivanje anti-HCV kontinuirano se unaprijeđuju unošenjem dodatnih antigenskih komponenti (testovi prve, druge, treće generacije).
Anti-HCV se mogu najranije detektirati (6-8 tjedana) testovima treće generacije imunoenzimskih testova (EIA). U serumu bolesnika prvo se pojavljuju protutijela usmjerena na NS3 regiju (anti-c33) i antigen nuklekapside (anti-c22), a poslije na NS4 regiju te na E1 i E2 (79). Specificnost EIA testova iznosi više od 99% (92, 95). No buduci da su moguci lažno pozitivni rezultati, svaki pozitivan nalaz EIA testa potrebno je potvrditi tzv. potvrdnim testovima. U skupinama niskog rizika za HCV infekciju lažno pozitivan rezultat se nade u 25- 90% bolesnika, dok u skupinama visokog rizika lažan pozitivitet iznosi oko 5-10%. Najčešce upotrebljavani potvrdni testovi za dijagnostiku HCV su western blot te imunoblot (RIBA, engl. recombinant immunoblot assay) kojima je moguce dokazati specificna protutijela na svaki pojedini antigen HCV. Analizom njihove dinamike moguce je pratiti njihovu pojavu u serumu, trajanje i nestajanje.
Nalaz anti-HCV protutijela u serumu dokaz je kontakta s HCV. Medutim, u oko 15% bolesnika inficiranih s HCV dolazi do spontane eliminacije virusa te nalaz protutijela ne znaci infekciju, vec imunološki učinkovit kontakt s HCV. Za potvrdu postojanja infekcije nužno je dokazivanje HCV-RNA.
7.2. Molekularna dijagnostika infekcije virusom hepatitisa C
Genom virusa (HCV-RNA) pojavljuje se u krvi rano tijekom infekcije, već oko 14. dana od ulaska virusa u organizam. HCV-RNA je prisutna u krvi tijekom akutne i kronične infekcije i jasan je dokaz HCV infekcije. Za detekciju HCV-RNA najcešce se koristi molekularna metoda koja kombinira reverznu transkripciju virusne RNA i PCR (RT-PCR). Molekularnim se metodama može dokazati akutna infekcija u vrijeme tzv. “imunološkog prozora”, tj. prije serokonverzije. Osim kvalitativnih testova, postoje i kvantitativni testovi kojima se određuje kolicina HCV-RNA u serumu – tzv. virusno opterecenje (engl. “viral load”) što je osobito korisno za praćenje učinka terapije. Granica osjetljivosti ovih testova iznosi 50 internacionalnih jedinica (IU) HCV-RNA/ml seruma.
Vrlo važna značajka akutne HCV infekcije je “varijabilnost” razine HCVRNA od nekoliko stotina do 1 000 000 IU/mL, a neki bolesnici imaju intermitentno negativan PCR nalaz. Na temelju tih fluktuacija može se razlikovati akutna od kronične HCV infekcije kod koje je razina HCV-RNA stabilna i ne mijenja se više od jednog dekadskog logaritma.
7.3. Odredivanje genotipa virusa hepatitisa C
Odredivanje genotipa HCV važno je zbog epidemiološkog pracenja, ali poglavito
zbog razlicitog odgovora na standardno lijecenje. Za odredivanje genotipa
HCV primjenjuje se nekoliko metoda:
1) PCR hibridizacijska metoda, koja se zasniva na amplifikaciji genoma
te se potom PCR produkt veže (hibridizira) uz genotip specificne oligonukleotidne
probe nanesene na nitrozocelulozne trake;
2) PCR restrikcijska metoda koja ukljucuje PCR te nakon toga restrikciju
enzimima koji cijepaju PCR produkt na genotip-specificnim mjestima. Rezultati
se očitavaju nanošenjem produkata na agarozni gel obojen etidi bromidom
i izložen UV svjetlu;
3) Metoda sekvenciranja kojom se odreduje nukleotidni slijed PCR produkta.
7.4. Dodatni moguci biljezi infekcije virusom hepatitisa C
Hepatitis C core antigen (HCVAg)
HCVAg pojavljuje se u krvi gotovo istodobno s HCV-RNA (može se detektirati 1-2 dana nakon HCV-RNA) i prisutan je oko dva mjeseca (79). EIA testom moguće je odrediti slobodni HCV Ag (u ranoj fazi infekcije, kada još nema protutijela) i vezani HCV (kompleks HCVAg/anti-HCV). S obzirom da perzistira ograničeno vrijeme i ima jasnu dinamiku, može poslužiti kao biljeg akutne infekcije. Određivanjem HCVAg u anti-HCV pozitivnih osoba može se odrediti je li došlo do eliminacije virusa ili je on i dalje prisutan, dok pri anti-HCV negativitetunalaz HCVAg u periodu “imunološkog prozora” jasno ukazuje na akutnu HCV infekciju. Odredivanje HCVAg osobito je važno u imunokompromitiranih bolesnika zbog “nestajanja” anti-HCV te ponovne pojave HCVAg koji više nije vezan u HCVAg/anti-HCV kompleksu.
Anti-HCV IgM protutijela
Iako se IgM anti-HCV nalaze u gotovo svih akutnih HCV infekcija, u visokom se postotku (više od 80%) nalaze i u kroničnoj HCV infekciji te se ne mogu koristiti kao biljeg akutne infekcije. Mogu se koristiti za procjenu uspješnosti terapije te za razlikovanje reakcije odbacivanja od reinfekcije s HCV u transplantiranoj jetri. Ima izvještaja da u dijagnostici akutne HCV infekcije može koristiti određivanje titra IgM protutijela koji je u prosjeku znatno viši od onog u kroničnoj HCV infekciji, no određivanje ovih protutijela ne smatra se dovoljno pouzdanim za rutinsku dijagnostiku.
IgG avidnost
U novije se vrijeme u dijagnostici HCV infekcije odreduje i avidnost IgG protutijela. Opaženo je da osobe s HCV infekcijom u kojih je došlo do eliminacije virusa imaju niže vrijednosti IgG aviditeta u odnosu na osobe s kronicnom HCV infekcijom.
8. LIJEČENJE HEPATITISA C
Suvremena terapija hepatitisa C sastoji se od kombinirane primjene pegiliranog
interferona i ribavirina. Mehanizam djelovanja interferona sastoji se
u sprečavanju vezanja virusa na stanice, indukciji proteinske kinaze koja
inhibira sintezu proteina fosforilacijom inicijacijskog faktora translacije
(eIF2a), smanjenju razine virusne RNA te stimulaciji citotoksicnih limfocita
T i NK stanica.
Pegilirani interferon je kemijski modificirani rekombinantni interferon dobiven kovalentnim vezanjem inertnog polietilen-glikola (PEG) s interferonom. Tim je postupkom produljeno njegovo vrijeme poluživota, a time i njegova učinkovitost. U kliničkom se lijećenju koriste dva oblika pegiliranog interferona: a-2a i a-2b. Limfoblastoidni interferon je prirodni interferon koji se proizvodi iz humanih limfoidnih stanicnih linija i sadrži multiple podtipove interferona-a. Konsenzusni interferon dobiven je skeniranjem a-interferonskih podtipova te konstruiranjem konsenzus molekule koja na svakoj poziciji ima najcešce opaženu aminokiselinu. Sekvenca koja kodira DNA sintetizirana je na osnovi konsenzusne sekvence, a molekula je klonirana u rekombinantnom sistemu E.coli.
Ribavirin je analog guanozina koji inhibira umnožavanje nukleotidne sekvence RNA i DNA virusa. Mehanizmi djelovanja ukljucuju smanjenje intracelularnog trifosfata izravnom inhibicijom inozin monofosfat dehidrogenaze te inhibiciju RNA polimeraze.
Tablica 5. Oblici interferona koji se primjenjuju u lijecenju hepatitisa
C
O lijecenju akutnog hepatitisa C još nema jasnog stava. U literaturi se trenutno preporučuje lijecenje pegiliranim interferonom-a u trajanju od 8-12 tjedana. U liječenju kroničnog hepatitisa C preporučuje se pegilirani interferon-a i ribavirin. Duljina liječenja ovisi o genotipu i iznosi 48 tjedana za genotipove 1 i 4 te 24 tjedna za genotipove 2 i 3. Lijecenje se preporučuje za osobe s trajno povišenim vrijednostima transaminaza te histološki potvrdenom aktivnom bolesti jetre, osobito uz postojanje fibroze.
U ispitivanju su i mnogobrojni novi lijekovi kao inhibitori HCV proteaze (ACH 808, SCH 503034), inhibitori HCV polimeraze (HCV-759, HCV-796, R-1626, R 7128), albumin interferon, nukleozidni inhibitori (MK-06080) te analog ribavirina taribavirin.
LITERATURA
1. Burek V. Laboratorijska dijagnostika virusnih hepatitisa B i C. Acta Med Croatica 2005; 59(5):405-12.
2. Grahovac B, Hadžisejdic I. Molekularna dijagnostika hepatitisa C. Medicina 2006; 42:132-7.
3. Mihaljević I. Serologic diagnosis of viral hepatitis A-E. Biochemia Med 2000:10:161-73.
4. Shepard CW, Finelli L, Alter MJ. Global epidemiology of hepatitis C virus infection. Lancet Infect Dis 2005; 5(9):558-67.
5. Stanković-Đorđević D, Otašević M, Tasić G, Dinić M, Miljković-Selimović B. Hepatitis C virusna infekcija virusološki i patofiziološki apekt. Acta Medica Mediana 2002;42(1)1:43-52.
6. Vince A. Hepatitis B i C: prirodni tijek bolesti. Acta Med Croatica 2005; 59:389-92.
7. Vince A. Virusni hepatitis kao spolno prenosiva bolest. Medicus 2003; 12(2):231-6.
8. Vucelić B, Hrstić I, Begovac J, i sur. Virusni hepatitis: hrvatska konsenzus konferencija. Acta Med Croatica 2005; 59:359-75.
preuzmi
seminarski rad u wordu » » »
